Eficacia
La eficacia a largo plazo de Brintellix® en pacientes con trastorno depresivo mayor (TDM)
Hasta 1 de cada 4 personas que se recuperan de un episodio depresivo mayor experimentará una recurrencia dentro del primer año2. Además, una mayor cantidad de episodios previos, una mayor duración del episodio depresivo mayor y síntomas depresivos más graves suelen predecir recurrencias futuras3.
Para prevenir la recaída y la recurrencia, se recomienda un tratamiento a largo plazo de al menos seis meses después de la remisión del episodio depresivo agudo para pacientes con TDM que hayan respondido al tratamiento agudo3,4.
Los datos de cinco estudios a largo plazo, a etiqueta abierta, de extensión de dosis flexible, evaluaron si las mejoras en los síntomas depresivos del TDM continúan después del tratamiento agudo (de seis a ocho semanas) con Brintellix®1.
Observe los hallazgos a continuación.
Brintellix® (5-20 mg) brinda un alivio sostenido de los síntomas del TDM† a largo plazo1,5
Cambio en la puntuación total MADRS en pacientes tratados previamente con 5-20 mg al día de Brintellix® en ensayos controlados (agudos) que continuaron el tratamiento en estudios de extensión a etiqueta abierta durante 52 semanas1.
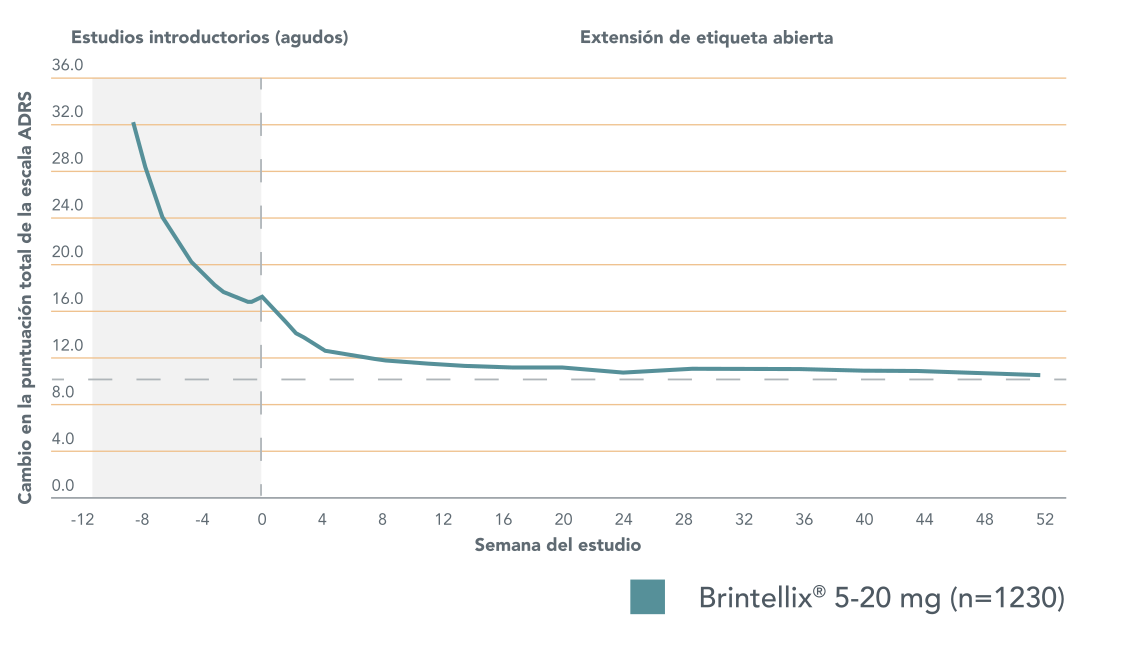
Adaptado de Vieta E et al. 2017.
La línea discontinua horizontal indica el punto de corte para la remisión (definida por una puntuación total de MADRS ≤10).
La línea discontinua vertical representa el inicio del tratamiento en el estudio de extensión.
Las mejoras en los síntomas del TDM† observadas con Brintellix® durante los estudios a corto plazo (6-8 semanas) continuaron al inicio del estudio de extensión y se mantuvieron con el tratamientocontinuo durante 52 semanas1.

Se demostró que Brintellix® fue generalmente bien tolerado a largo plazo1 y que tuvo un perfil de seguridad consistente con estudios clínicos previos5.6. El evento adverso emergente del tratamiento informado con mayor frecuencia fue náusea (16.6%). Otros eventos adversos con una incidencia de ≥5% incluyeron dolor de cabeza (12.9%), nasofaringitis (9.4%), diarrea (6.4%) y aumento de peso (5.3%)1. La tasa de abandono durante la extensión a largo plazo debido a cualquier evento adverso fue baja (7.8%)1.
† Según la medición de la escala MADRS.
‡ Basado en la incidencia de síntomas de discontinuación (medidos según la escala DESS) y tasas de
abandono debido a eventos adversos emergentes del tratamiento5,6.
Abreviaturas:
MADRS, escala de puntuación de la depresión de Montgomery-Åsberg; TDM, trastorno depresivo mayor.

